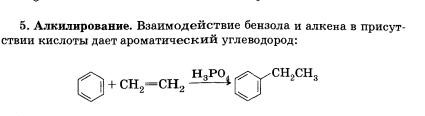
Задача 29347 29) Рассчитайте массу (кг) продукта,...
Условие
химия 10-11 класс
9936
Решение
★
m(C6H6)=776 кг= 776000 г
V(C2H4)=200 м^(3)=200000 л
(1 л = 1 дм^(3) = 0.001 м^(3) )
n(C6H6)=m/M=776000/(12*6+6)=776000/78=9948.7 моль
n(C2H4)=V/V_(m)=200000/22.4=8928.6 моль
Этилен находится в недостатке, значит это лимитирующий компонент реакции, по которому мы будем проводить дальнейшие вычисления.
По уравнению реакции, сколько вступило в реакцию этена, столько и образуется этилбензола.
n(C6H5-(C2H5))=8928.6 моль
m(C6H5-(C2H5))=n*M(C6H5-(C2H5))=8928.6*(78+24+4)=106*8928.6=946431 г =946 кг
Ответ: 946 кг