Задача 80166 ...
Условие
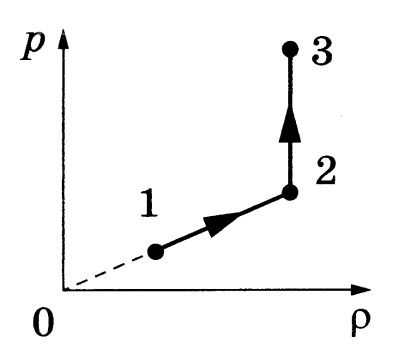
Решение
ρ= m /V , V = m /ρ .
Для идеального газа pV = nRT (n = const)
⇒ T = μp /(ρR) = p /(ρR* ) ,
где R* = R/μ – газовая постоянная в пересчёте на 1 кг.
Первый закон термодинамики
dQ = dU + p dV = c v dT + p dV . (1)
Перепишем (1) через ρ вместо V.
dV = – V dρ /ρ = – (1/ρ²) dρ , p dV = – p dρ /ρ² .
Подставляя T(p,ρ) и c v =(3/2)R* (для одноатомного газа), получаем
dQ = (3/2)(dp /ρ) – (5/2)(p dρ /ρ²) (2)
или, деля на dρ ,
dQ∝ dp/dρ – (5/3)(p/ρ). (3)
Следовательно
• если dp/dρ > (5/3)(p/ρ) , то dQ >0 – газ получает тепло;
• если dp/dρ < (5/3)(p/ρ) , то dQ <0 – газ отдаёт тепло.
Заметим, что условию dQ =0 соответствует
dp/dρ = (5/3)(p/ρ) ,
т. е. кривая адиабаты (pρ –γ = const, γ = 5/3) действительно граничит области «получает/отдаёт теплоту».
Процесс 1–2
На диаграмме p–ρ от точки 1 к 2 давление растёт не слишком круто: наклон линии меньше, чем у адиабаты, проходящей через точку 1 (адиабата круче, потому что γ = 5/3 >1).
Следовательно
dp/dρ < (5/3)(p/ρ) → dQ <0 .
Значит, при переходе 1–2 газ ОТДАЁТ теплоту (Q12<0).
Физически: газ сжимается (V уменьшается, A<0); работа внешних сил повышает его внутреннюю энергию, однако часть этой работы уходит наружу в виде теплоты.
Процесс 2–3 (ρ = const)
V = const ⇒ p dV =0 ⇒ A23 =0.
При росте p температура (и внутренняя энергия U = (3/2)nRT) увеличивается, ΔU>0.
По первому закону Q23 = ΔU >0 – газ ПОЛУЧАЕТ теплоту.
Итог
• в участке 1–2 газ отдаёт тепло (Q12 < 0);
• в участке 2–3 газ получает тепло (Q23 > 0).